A oxidação livre ocorre com a participação de formas radicais livres de oxigênio, que são formadas no processo de redução de um elétron do oxigênio e, acima de tudo, superóxido ânion oxigênio.
Normalmente, essas reações de oxidação radical ocorrem no centro ativo das enzimas correspondentes e os produtos intermediários não aparecem no ambiente externo. Quando as condições de funcionamento da cadeia respiratória mudam (por exemplo, durante a hipóxia), nela também é possível a redução de um elétron do oxigênio, devido ao fato de sua afinidade pela ubiquinona ser maior do que pela citocromo oxidase. Esses processos levam à formação de ânion superóxido de oxigênio. Esse radical também pode ser formado sob a influência dos raios ultravioleta, bem como pela interação do oxigênio com íons metálicos de valência variável (na maioria das vezes com ferro) ou durante a oxidação espontânea de certos compostos, como a dopamina. Finalmente, pode ser produzido nas células por enzimas como a xantina oxidase ou a NADPH oxidase.
A formação do ânion superóxido de oxigênio tem importante significado biológico. É um composto altamente reativo que, devido à sua alta hidrofilicidade, não consegue sair da célula e se acumula no citoplasma. Suas transformações levam à formação de vários agentes oxidantes ativos (Fig. 9.10). É capaz de ativar a NO sintase, que forma um radical NO nos tecidos, que possui propriedades de segundo mensageiro (ativa a guanilato ciclase solúvel, cujo produto, cGMP, apresenta propriedades vasodilatadoras). Por outro lado, o ânion superóxido é capaz de reduzir o conteúdo do radical NO, convertendo-o em peroxinitrito ONOOH (ver Fig. 9.10).
As células vivas possuem sistemas de defesa contra o aumento da produção de radicais livres. Enzima superoxido dismutação converte o ânion superóxido do oxigênio no peróxido de hidrogênio menos reativo e mais hidrofóbico H2SOBRE2. O peróxido de hidrogênio é um substrato para peroxidases dependentes de catalase e glutationa, que catalisam sua conversão em uma molécula de água. No entanto, o peróxido de hidrogênio pode gerar um radical hidroxila na presença de ferro ferroso ou ser convertido no ânion hipoclorito OCl pela enzima mieloperoxidase.
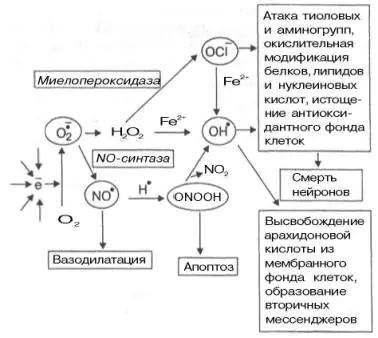
Arroz. 9.10. Interconversões de radicais livres e suas principais funções nos tecidos [Boldyrev A.A., 1996].
Tanto o ânion hipoclorito quanto o radical hidroxila são fortes agentes oxidantes. Eles são capazes de modificar proteínas, ácidos nucléicos, induzir a peroxidação lipídica (da qual os lipídios da membrana poliinsaturados mais “sofrem”) e, como resultado de reações em cadeia, levar a múltiplos danos à membrana e morte celular. Um acréscimo importante a essas reações é a capacidade do radical NO, ao interagir com o ânion superóxido, de formar peroxinitrito, que pode induzir a chamada apoptose (morte celular programada), e durante sua decomposição espontânea, transformar-se em radical hidroxila. Este último também pode ser formado a partir do ânion hipoclorito na presença de íons de ferro.
Os processos que ocorrem antes da formação do ânion hipoclorito ou do radical hidroxila estão localizados no citoplasma e são controlados por enzimas citoplasmáticas ou antioxidantes naturais solúveis em água. Por exemplo, taurina capaz de se ligar ao ânion hipoclorito na forma de um complexo de cloramina, um dipeptídeo carnosina e seus derivados neutralizam o radical hidroxila, e compostos como proteínas ferritina, ligue o ferro. A peroxidação lipídica, iniciada no espaço hidrofóbico das membranas celulares, é capaz de interromper o conhecido antioxidante hidrofóbico α-tocoferol (vitamina E). A sua elevada concentração nas membranas biológicas evita que sejam danificadas pelos radicais livres.
A supressão completa dos processos de peróxido nos tecidos é aparentemente impraticável; os radicais livres têm propriedades benéficas. Induzem a apoptose e participam na formação da imunidade celular. A formação de hidroperóxidos das cadeias de ácidos graxos dos fosfolipídios poliinsaturados danifica a bicamada e, ao estimular o trabalho das fosfolipases, promove a liberação de ácidos graxos dos lipídios da membrana. O ácido araquidônico poliinsaturado é um alvo comum para o ataque dos radicais livres. Este processo pode estimular suas transformações enzimáticas de duas maneiras - lipoxigenase ou ciclooxigenase. Como resultado, importantes reguladores biológicos são formados na célula: prostaglandinas, leucotrienos, tromboxanos. Os lisofosfolipídios formados durante a clivagem de um ácido graxo modificado podem ser restaurados ao seu estado original usando outro ácido graxo (na forma de acil-CoA). Desta forma, a composição de ácidos graxos das moléculas lipídicas na membrana celular pode ser regulada.
Radicais livres de oxigênio altamente reativos, caracterizados por alto potencial de oxidação e capacidade de sofrer transformações rápidas, podem induzir reações em cadeia. Atualmente, é reconhecido o importante papel dos processos de radicais livres no desenvolvimento de condições patológicas e relacionadas à idade nos tecidos [Vladimirov Yu.A. et al., 1983]. As transformações dos radicais livres estão envolvidas em mecanismos que aumentam a sobrevivência celular em condições desfavoráveis, e a diminuição da geração de radicais livres no organismo contribui para o enfraquecimento da imunidade celular. No entanto, o aumento da geração de radicais livres acompanha condições patológicas (doença de Parkinson, doença de Alzheimer) e o próprio processo de envelhecimento biológico.
NÍVEL DE GERAÇÃO DE RADICAIS LIVRES EM AMOSTRAS DE EJACULAÇÃO DE PACIENTES COM INFERTILIDADE
O nível de geração de radicais livres em amostras de ejaculação de pacientes inférteis foi avaliado pelo método de quimioluminescência. Foi demonstrado que em amostras contendo anticorpos anti-espermatozoides, a probabilidade de danos à membrana plasmática do esperma aumenta devido à geração excessiva de radicais livres. Muita atenção é dada ao estudo do papel dos anticorpos antiespermatozoides (ASAT) no processo reprodutivo. Contudo, a questão do efeito da ACAT na fertilização ainda permanece obscura. Os trabalhos de alguns autores revelam uma relação entre a presença de anticorpos e a diminuição da probabilidade de gravidez, enquanto em outros estudos questiona-se a influência do ACAT na diminuição deste indicador em pacientes com anticorpos. O objetivo deste trabalho foi avaliar o nível de geração de SR em amostras de ejaculado ACAT positivo e ACAT negativo.
Publicação: Boletim de Biologia Experimental e Medicina
Ano de publicação: 2001
Volume: 3s.
Informações adicionais: 2001.-N 6.-P.658-660
Visualizações: 171
Espécies reativas de oxigênio (ROS) – compostos nos quais o oxigênio possui um elétron desemparelhado.
As ERO são formadas quando as condições de funcionamento da cadeia respiratória mudam (por exemplo, durante a hipóxia), sob a influência dos raios UV, durante a interação do oxigênio com íons metálicos de valência variável (ferro), durante a oxidação espontânea de certas substâncias, com a participação das enzimas xantina oxidase ou NADPH oxidase. Nessas condições, é formado superóxido ânion oxigênio O2 .− , então peróxido de hidrogênio H2SOBRE2 E radical hidróxido HO. . Eles causam espécies reativas de oxigênio peroxidação lipídica - um processo que leva a graves danos à membrana, danificando proteínas e DNA.
A inativação de espécies reativas de oxigênio nas células ocorre sob a ação do sistema antioxidante. Inclui várias enzimas antioxidantes e antioxidantes de baixo peso molecular (vitamina C, glutationa, vitamina E, etc.).
Superoxido dismutação(SOD) converte o ânion superóxido de oxigênio em peróxido de hidrogênio H2SOBRE2:
Catalase - a enzima hemina contendo Fe 3+ catalisa a reação de decomposição do peróxido de hidrogênio. Isso produz água e oxigênio:
A maior atividade da catalase no corpo é característica do fígado. Há muita catalase nos eritrócitos. Lá ele protege a hemoglobina heme da oxidação.
Peroxidase- enzima heme, reduz o peróxido de hidrogênio a água; Ao mesmo tempo, outra substância é oxidada:
A peroxidase é capaz de decompor outros peróxidos, convertendo-os em álcoois. A atividade da peroxidase é encontrada no fígado, rins e leucócitos neutrofílicos.
Antioxidantes - substâncias biologicamente ativas que interagem com os radicais livres e previnem os processos de oxidação radicalar livre de substâncias orgânicas no corpo.
Vitaminas,exibindo propriedades antioxidantes - S, E, A, R. Tripeptídeo exibe propriedades antioxidantes glutationa, taurina (ácido 2-aminoetanossulfônico), dipeptídeo carnosina
A supressão completa dos processos de peróxido nos tecidos é aparentemente impraticável. Os radicais livres induzem apoptose, participe da formação imunidade celular, estimular o trabalho das fosfolipases, participando assim da síntese dos eicosanóides.
No entanto, o aumento da geração de radicais livres acompanha condições patológicas (doença de Parkinson, doença de Alzheimer) e o próprio processo de envelhecimento biológico.
Data adicionada: 19/03/2015; visualizações: 759; ENCOMENDE UM TRABALHO ESCRITO



